

| ความหมาย | แอลกอฮอล์(R - OH) | กรดอินทรีย์(R - COOH)
| สารอินทรีย์ที่มีหมู่ OH | กับหมู่ไฮโดรคาร์บอน สารอินทรีย์ที่มีหมู่ COOH | กับหมู่ไฮโดรคาร์บอน สูตรทั่วไป
| CnH2n+2O
| CnH2nO2
| การอ่านชื่อ
| พยางค์หน้าบอกจำนวน C อะตอม | พยางค์หลังบอกแอลกอฮอล์ ลงท้ายด้วย "ol" CH3OH Methanol CH2CH2OH Ethanol พยางค์หน้าบอกจำนวน C อะตอม | พยางค์หลังบอกกรดอินทรีย์ ลงท้ายด้วย "oic acid" CH3COOH Ethanoic acid CH3CH2CH2COOH Butanoic acid สมบัติ | 1.สถานะ ของแข็ง
| ของเหลว,ของแข็ง
| 2.การละลายน้ำ
| โมเลกุลเล็กละลายน้ำดี C1-C3โมเลกุลที่มี C มากขึ้น การละลายน้ำลดลง ไม่ละลายในที่สุด
| โมเลกุลเล็กละลายน้ำดี C1-C3โมเลกุลที่มี C มากขึ้น ละลายน้ำลดลง ถ้า C มากๆ ไม่ละลายน้ำ
| กรดอินทรีย์ละลายน้ำได้ดีกว่าแอลกอฮอล์ที่มี C เท่ากัน
| 3.แรงยึดเหนี่ยว | ระหว่างโมเลกุล พันธะไฮโดรเจนและแรงแวนเดอร์วาลส์ | โมเลกุลเกิดพันธะไฮโดรเจน 3 แห่ง พันธะไฮโดรเจนและแรงแวนเดอร์วาลส์ | 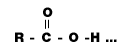 โมเลกุลเกิดพันธะไฮโดรเจน 5 แห่ง 4.ความเป็นกรด-เบส
| (กรด-เบส) แต่มีความเป็นกรดมากกว่าความเป็นเบส ภาวะปกติแอลกอฮอล์ไม่เปลี่ยนสีกระดาษลิตมัส
| กรดเปลี่ยนสีกระดาษลิตมัสจากน้ำเงินเป็นแดง
| 5.จุดเดือด(C ํ) | ซึ่งมวลโมเลกุล ใกล้เคียงกัน สูงปานกลาง
| สูงมาก
| จุดเดือดของสาร | พวกเดียวกันเอง เพิ่มขึ้นตามจำนวน C อะตอมที่เพิ่มขึ้น
| เพิ่มขึ้นตามจำนวน C อะตอมที่เพิ่มขึ้น
| 6.ความหนาแน่น
| น้อยกว่าน้ำเฉพาะโมเลกุลเล็ก
| มากกว่าน้ำส่วนใหญ่
| 7.ทำปฏิกิริยากับ | (หมู่ IA) 
(M = โลหะใดๆ ยกเว้นโลหะมีตระกูล) | ได้เร็ว เกิดก๊าซ H2 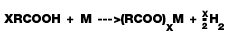
8.กลิ่น
| กลิ่นเฉพาะตัว(กลิ่นเหล้า)
| กลิ่นฉุน
| 9.ทำปฏิกิริยากับ | NaHCO3 ไม่ทำ
| 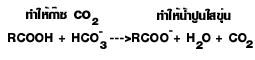
10.ทำปฏิกิริยากับ | แอลกอฮอล์ ไม่ทำ
| ทำให้เกิดเอสเทอร์ | (ต้องมีตัวเร่งปฏิกิริยา H2SO4(conc)) 11.ทำปฏิกิริยากับ | กรดอินทรีย์ ทำให้เกิดเอสเทอร์
| ไม่ทำ
| 12.จำนวนไอโซเมอร์
| C 3 อะตอมขึ้นไป | เกิดไอโซเมอร์พวกเดียวกันเอง C 4 อะตอมขึ้นไป | เกิดไอโซเมอร์พวกเดียวกันเอง จำนวน C อะตอมเท่ากันแอลกอฮอล์จะเกิดไอโซเมอร์กันเองได้มากกว่ากรออินทรีย์
| | ||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

