
สารละลายเป็นสารเนื้อเดียวที่ได้จากการผสมสารบริสุทธ์ตั้งแต่ 2 ชนิดขึ้นไปเข้าด้วยกัน ถ้าสารที่นำมาผสมกันมีสถานะเดียวกันจะถือว่าสารที่มีปริมาณมากที่สุดเป็นตัวทำละลาย ส่วนสารที่มีปริมาณน้อยกว่าเป็นตัวละลาย จุดเดือดของสารละลายสูงกว่าตัวทำละลายบริสุทธิ์ และจุดหลอมเหลวของสารละลายต่ำกว่าตัวทำทำละลายบริสุทธิ์ และถ้าสารละลายที่มีความเข้มข้นในหน่วยโมลต่อกิโลกรัมเท่ากัน จะมีจุดเดือดและจุดหลอมเหลวเท่ากัน โดยที่ตัวละลายจะเป็นสารใดก็ได้แต่ต้องเป็นสารที่ระเหยยากและไม่แตกตัวเป็นไอออน ส่วนสารละลายที่มีความเข้มข้นต่างกัน แม้จะมีตัวทำละละายชนิดเดียวกันก็มีค่าจุดเดือดและจุดหลอมเหลวไม่เท่ากัน
สูตรเกี่ยวกับสารละลายที่มีสมบัติคอลลิเกตีฟ
1. จุดเดือด
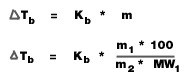
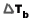 = จุดเดือดของสารละลาย - จุดเดือดของตัวทำละลาย (องศาเซลเซียส)
= จุดเดือดของสารละลาย - จุดเดือดของตัวทำละลาย (องศาเซลเซียส)
Kb = ค่าคงที่ของการเพิ่มขึ้นของจุดเดือดของสารละลาย (องศาเซลเซียส/mol/kg)
m = ความเข้มข้นของสารละลาย (mol/kg)
m1 = มวลตัวถูกละลาย (g)
m2 = มวลของตัวทำละลาย (g)
MW1 = มวลโมเลกุลของตัวถูกละลาย
2. จุดหลอมเหลว (หรือจุดเยือกแข็ง)
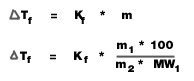
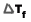 = จุดเยือกแข็งของตัวทำละลาย - จุดเยือกแข็งของสารละลาย (องศาเซลเซียส)
= จุดเยือกแข็งของตัวทำละลาย - จุดเยือกแข็งของสารละลาย (องศาเซลเซียส)
Kf = ค่าคงที่ของการลดลงของจุดเยือกแข็งของสารละลาย (องศาเซลเซียส/mol/kg)


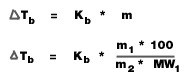
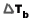 = จุด
= จุด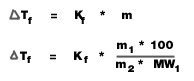
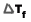 = จุด
= จุด